Atome sind bestrebt, in ihrer äussersten Schale die sogenannte Edelgaskonfiguration zu erreichen.
Hauptgruppen: Elektronen im Periodensystem
Im Periodensystem sind die Elemente so angeordnet, dass von einem zum nächsten die Anzahl Protonen um eines zunehmen. Das bedingt, dass auch die Elektronen von einem zum anderen Element um eines zunehmen.
Die Ordnungszahl gibt an, wie viele Elektronen bzw. Protonen ein Element insgesamt enthält.
Die Valenzelektronen
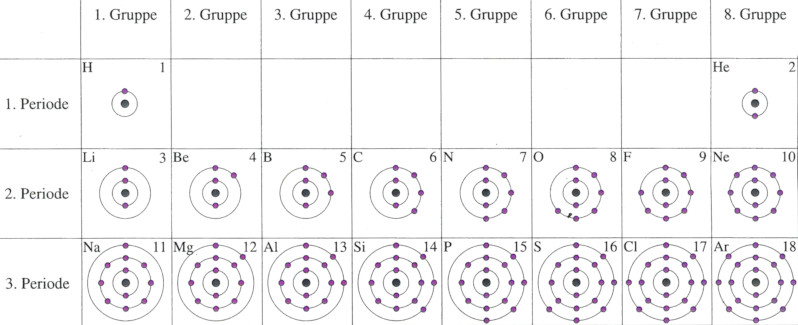
Edelgase
Beispiele von Edelgasen sind Helium, Neon, Argon und so weiter. Diese Elemente haben alle die Eigenschaft, dass sie sehr reaktionsträge sind. Grund dafür ist, dass ihre äusserste Schale, die Valenzschale, voll besetzt ist: Helium hat zwei Elektronen, Neon und Argon haben je acht.
Edelgaskonfiguration
Wenn die Valenzschale mit 8 Elektronen besetzt ist, spricht man von Edelgaskonfiguration. Dies kann von Nicht-Edelgasen durch Ionenbildung oder durch Elektronenpaarbindungen erreicht werden.